

肖林,研究员,博士生导师。2002年毕业于第二军医大学临床医学系,2007年获理学(神经生物学)博士学位,师从我国著名神经生理学家中国科学院院士陈宜张教授。2014至2016年间赴英国伦敦大学学院(UCL)英国皇家学会院士William D Richardson教授实验室进行工作。长期从事胶质细胞功能与相关脑疾病研究,尤其是少突胶质细胞的生理功能与发育调控,及其在脱髓鞘性疾病、神经退行性疾病和神经精神疾病中的作用和机制研究。主要运用动物行为学、多通道电生理记录、光遗传技术、分子生物学和形态学分析等综合实验手段。在《Science》等国际重要学术刊物发表 SCI原始论著多篇,其中以第一和/或通讯作者在《Nat. Neurosci.》(单篇引用380多次)、《Glia》、《J. Biol. Chem.》、 《Mol. Endocrinol》、《Endocrinology》等杂志发表论文10余篇。论文总计已被他引1800余次。主持(完成)国家自然基金面上项目5项,上海市基金3项,国家科技创新2030—“脑科学与类脑研究”重大项目研究骨干,广东省“脑科学与类脑研究”重点领域研发计划项目研究骨干。入选上海市“青年科技启明星”计划(A类)、上海市“浦江人才计划”(A类),解放军总后勤部优秀“青年科技人才扶持对象”,广东省“杰出青年卫生人才”等人才计划。获国家科技进步二等奖、军队科技进步一等奖,上海市科技进步二等奖、长三角神经科学青年科学家奖等奖励。
![]()
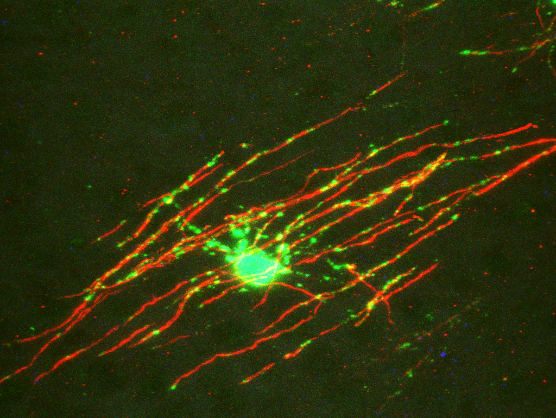
胶质细胞的数量占据了人脑神经细胞约半壁江山。然而,在近代以来的神经科学研究史上,它们的功能却长期被人们所忽视。最近一二十年来,越来越多的研究表明,胶质细胞远非其得名时所被赋予的大脑中“胶水”与“填充”之意,它实际上非常活跃地参与到了神经系统的正常生理活动,对神经功能的实现起到重要的调节,而它们的损伤或功能异常很可能导致诸多的神经甚至精神功能的障碍。因此,对胶质细胞功能的深入研究很可能为重新认识以往多年未解的诸多神经及精神疾病之谜打开新的窗口,并为这些疾病的预防、诊断和治疗提供新的思路与方向。
肖林研究员课题组长期从事胶质细胞功能与相关脑疾病研究,尤其是少突胶质细胞的生理功能与发育调控,及其在脱髓鞘性疾病、神经退性疾病和神经精神疾病中的作用和机制研究。
课题组主要以“胶质细胞在脑功能与脑疾病中的作用”为研究方向,以转基因小鼠、细胞及脑片培养,以及人脑标本为实验对象,采用生化及组织形态学分析,核磁共振影像、电生理及光遗传学等多种先进的技术方法,将重点关注但不限于以下科学问题的探索:
①少突胶质及其前体细胞(OPC)的生理功能,尤其是对神经环活性的调控及机制;
②人类中枢再髓鞘化失败的关键原因,以促进再髓鞘化为目的的相关疾病新型治疗途径的开发;
③少突胶质细胞在成体和发育期的新生调控异常或功能异常在自闭症、抑郁症、精神分裂症等精神疾病中的作用及机制;
④胶质细胞-神经元相互作用机制及其对神经功能和环路的影响。
课题组所在的单位建有先进的脑成像实验室,分子、细胞神经生物学实验室,同时正在积极建设高标准的动物行为实验室,拥有核磁共振仪,脑电记录及刺激仪,双光子显微镜等先进实验设备。拥有包括国家自然杰出青年基金获得者在内的教授或研究员10名,博导10名。形成了以揭示脑认知功能的神经机制为主体协同攻坚研究方向,同时在脑重大疾病机制研究放下发力的总体学科发展布局。尤其具有特色优势的是,研究院与广东三九脑科医院签署深度合作协议,共同建设联合研究中心,已经建立并在进一步扩大具有完全自主权的标准人脑组织库库(目前人脑病理标本数已超过1000例)及超大样本量的临床患者随访库,为开展从宏观脑功能fMRI到介观的神经环路再到微观的分子基因机制不同层面的一体化协同研究奠定了厚实的基础。
课题组常年招收青年英才博士后,同时热忱欢迎有志于神经科学的同学报考本组硕士博士研究生。欢迎来信咨询。liuyangxiaolin@aliyun.com

1997.9-2002.6 第二军医大学临床医学专业 获学士学位
2002.9-2007.6 第二军医大学神经科学研究所 硕博连读, 获博士学位
(导师:中科院院士陈宜张教授)
![]()
2007.7-2010.8 第二军医大学神经科学研究所 讲 师
2010.8-2018.12 第二军医大学神经科学研究所 副教授,硕导
2014.2-2016.6 University College London (UCL) Research Associate
(合作导师:英国皇家学会院士William D Richardson教授)
2019.1至今 华南师范大学脑科学与康复医学研究院 研究员, 博导
![]()
中国神经科学学会胶质细胞分委会委员
上海市康复医学会神经康复学专业委会常务理事
广东省神经科学学会理事
中国神经科学学会会员
中国生理学会会员
![]()
l 国家自然科学基金面上项目(No. 31970913):内源性糖皮质激素对少突胶质细胞新生和髓鞘形成与修复的调控及机制, 58万元(直接经费),2020.01-2023.12
l 国家自然科学基金面上项目(No.31471013):CC3通过调控olig1入核抑制OPC分化和髓鞘形成与再生,85万元,2015.01-2018.12
l 国家自然科学基金青年-面上连续项目(No.31270025):NMDA受体在少突胶质前体细胞分化和髓鞘化/再髓鞘化中的作用;85万元,2013.01-2016.12
l 国家自然科学基金青年项目(No.30900431):NMDA促进寡突胶质前体细胞(OPC)迁移的作用及机制;19万元,2010.01-2012.12
l 广东省“脑科学与类脑研究” 重点领域研发计划 “专题二: 脑疾病治疗关键技术研究(参与子课题:研发神经再生新技术)(项目号:2018B030332001)项目参与人,总经费3456万, 2019.01-2023.01
l 广东省“脑科学与类脑研究” 重点领域研发计划 “专题五: 自闭症诊治方法研究(参与子课题:自闭症的致病基因鉴定、动物模型构建及病理机制解析)(项目号:2019B030335001)项目参与人,总经费3980万元,2019.09-2023.09
l 华南师范大学高水平大学建设专项资金高层次引进人才科研启动经费,项目负责人, 200万元人民币, 2019.01-2022.12
l 上海市浦江学者人才计划(No.17PJ1410900):少突胶质细胞新生与中枢再髓鞘化调控,20万元,2017.07-2019.06
l 中国人民解放军总后勤部优秀青年科技人才扶持基金:髓鞘形成与再生调控;10万元,2013.01-2015.12
l 上海市科技启明星计划(A类,No.12QA1404200):CC3调控少突胶质前体细胞分化和髓鞘化/再髓鞘化的作用及机制;20万元,2012.09-2014.08
l 上海市卫生局青年基金(20114Y185):Diosgenin促进少突胶质前体细胞分化与髓鞘再生的作用及机制;2万元,2011.1-2012.12
l 第二军医大学优秀青年学者基金:髓鞘发育与再生机制研究;12万元,2011.10-2015.12
l 第二军医大学青年启动基金:甾体激素对寡突胶质前体细胞(OPC)生物学性状的调节及机制研究;5万元,2007.12-2009.12
l 第二军医大学博士创新基金:糖皮质激素非基因组作用参与调解神经元兴奋毒性损伤;4万元,2005.9-2007.6

l 广东省杰出青年卫生人才(2019)
l 长三角地区神经科学青年科学家奖(2017)
l 上海市浦江学者人才计划(A类,2017)
l 军队科技进步一等奖(2020,R12/14)
l 上海市科技进步二等奖(2013,R10/10)
l 上海市科技启明星计划 (A类,2012)
l 中国人民解放军总后勤部优秀青年科技人才扶持对象 (2012)
l 第二军医大学优秀青年学者 (2011)
l 中国神经科学学会“赛诺菲-安万特”优秀论文奖 (2011)
l GSK-神经科学“明日之星”奖 (2011)
l 中国生理学会第十一届张锡均全国生理学青年优秀论文奖 (2011)
l 第二军医大学基础部优青年教师(2010)
l 第二军医大学基础部优秀党员(2010)
l 第二军医大学基础部嘉奖(2010)
l 第二军医大学“5511”优秀青年人才(2009)
l 第二军医大学先进教学个人(2008)
l 上海市优秀博士学位论文(2008)
1) Guo DZ#, Xiao L#, Liu YJ, Shen C, Lou HF, Lv Y, Pan SY*. Cathepsin D deficiency delays central nervous system myelination by inhibiting proteolipid protein trafficking from late endosome/lysosome to plasma membrane. Exp. Mol. Med. 2018, 50(3): e457. doi: 10.1038/emm.2017.291.( IF=5. 587,被引4次)
2) Xiao L#, Ohayon D#, McKenzie I, Sinclair-Wilson A, Wright JL, Fudge AD Emery B, Li HL, Richardson WD*. (2016), Rapid production of new oligodendrocytes is required in the first few hours of motor learning. Nat. Neurosci., 2016, 19(9):1210-7. doi: 10.1038/nn.4351. (IF=19.9,被引190次).
3) Marques S#, Zeisel A#, Codeluppi S, van Bruggen D, Mendanha Falcão A, Xiao L, Li H, Häring M, Hochgerner H, Romanov RA, Gyllborg D, Muñoz Manchado A, La Manno G, Lönnerberg P, Floriddia EM, Rezayee F, Ernfors P, Arenas E, Hjerling-Leffler J, Harkany T, Richardson WD, Linnarsson S*, Castelo-Branco G*. Oligodendrocyte heterogeneity in the mouse juvenile and adult central nervous system. Science. 2016, 352 (6291):1326-9. doi: 10.1126/science.aaf6463 (IF=41.2,被引342次).
4) Yang W#, Xiao L#, Li C, Liu X, Liu M, Shao Q, Wang D, Huang A, He C*. TIP30 Inhibits Oligodendrocyte Precursor Cell Differentiation via Cytoplasmic Sequestration of Olig1. Glia. 2015, 63(4):684-98. doi: 10.1002/glia.22778. (IF=6.2,被引11次)
5) Xiao L#, Hu C#, Guo DZ, Shen WR, Li C, Yang WJ, Liu XY, Huang AJ, Wang D, He C*, NMDA Receptor Couples Rac1-GEF Tiam1 to Direct Oligodendrocyte Precursor Cell Migration. Glia, 2013, 61(12):2078-99. (IF=6.2,被引37次)
6) Li C#, Xiao L#, Liu XY, Yang WJ, Shen WR, Hu C, Yang G, He C*. A functional role of NMDA receptor in regulating the differentiation of oligodendrocyte precursor cells and remyelination, Glia, 2013, 61(5): 732-749. (IF=6.2,被引103次)
7) Xiao L#, Guo DZ#, Hu C, Shen WR, Shan L, Li C, Liu XY, Yang WJ, Zhang WD*, He C*. Diosgenin promotes oligodendrocyte progenitor cell differentiation through estrogen receptor-mediated ERK1/2 activation to accelerate remyelination. Glia, 2012, 60(7):1037-52. (IF=6.2,被引57次)
8) Liu M#, Xiao L#, Liu S, Hu Y, Tian J, Gao G, Xie S, Guan Y*. Immunoregulation of myelin-specific CD4(+) T cell response by neural stem/progenitor cells: Role of prostaglandin E2. J Neuroimmunol. 2013, 255(1-2):32-8. (IF=3.024,被引5次)
9) Xiao L*, Hu C, Feng CZ, Chen YZ*. Switching of N-methyl-D-aspartate (NMDA) receptor-favorite intracellular signal pathways from ERK1/2 to p38 MAPK leads to developmental changes in NMDA neurotoxicity. J Biol Chem. 2011, 268(23): 20175-20193. (IF=5.117,被引34次)
10) Xiao L*, Feng CZ, Chen YZ*. Glucocorticoid rapidly enhances NMDA-evoked neurotoxicity by attenuating the NR2A-containing NMDA receptor-mediated ERK1/2 activation. Mol Endocrinol. 2010, 24(3):497-510. (IF=4.816,被引59次)
11) Xiao L, Qi AQ, Chen YZ*. Cultured embryonic hippocampal neurons deficient in glucocorticoid (GC) receptor: a novel model for studying nongenomic effects of GC in the neural system. Endocrinology, 2005, 146 (9): 4036-41. (IF=5.33,被引39次)
12) Xiao L Chen YZ*: Culture condition and embryonic stage dependent silence of glucocorticoid receptor expression in hippocampal neurons. J Steroid Biochem. Mol. Biol., 2008, 111: 147-155. (IF=3. 985,被引9次)
13) Wang W, Gao XF, Xiao L, Xiang ZH, He C*. KV7/KCNQ Channels are functionally expressed in oligodendrocyte progenitor cells. PLoS ONE, 2011 6(7): e21792. (IF=4.61,被引18次)
14) Liu SJ, Yu M, He Y, Xiao L, Wang F, Song CC, Sun SH*, Ling CQ*, Xu ZH*. Melittin prevents liver cancer cell metastasis through Inhibition of the Rac1-dependent pathway, Hepatology, 2008, 47(6): 1965-1973. (IF=11.044,被引191次)
15) Li YX, Ding SJ, Xiao L, Guo W, Zhan Q*. Desferoxamine preconditioning protects against cerebral ischemia in rats by inducing expressions of hypoxia inducible factor 1α and erythropoietin. Neurosci. Bulletin, 2008, 24 (2):89-95. (IF=1.313,被引57次)
16) Yang HY, Yu JP, Fu G, Shi XY, Xiao L, Chen YZ, Fang XH*, He C*. Interaction between single molecules of Mac-1 and ICAM-1 in living cells: an atomic force microscopy study. Exp. Cell Res., 2007, 313(16):3497-504. (IF=3.787,被引50次)
17) Qi AQ, Qiu J, Xiao L, Chen YZ*: Rapid activation of JNK and p38 by glucocorticoids in primary cultured hippocampal cells. J Neurosci. Res., 2005, 80 (4):510-7. (IF=3.378,被引71次)
18) Qi AQ, Qiu J, Xiao L, Chen YZ*: Rapid activation of ERK1/2 by glucocorticoids in primary cultured hippocampal cells. Prog. Nat. Sci., 2005,14(7):760-766. (IF=0.228)
19) Li XY, Qiu J, Xiao L, Zhu JQ, Chen YZ*: Rapid activation of p38 mitogen protein kinase by corticosterone in PC12 cells. Acta Physiologica Sinica, 2001, 53 (6):414-418.(被引7次)
20) 杨光,杨文静,李翠,张溢凡,肖 林(通讯作者),MicroRNA调控少突胶质细胞分化的研究进展, 生命的化学,2012, 2013,25(3):300-505。(综述)
21) 蔡沅锜,石长贵,肖 林(通讯作者),少突胶质前体细胞迁移调控分子研究进展,卒中与神经疾病,2011,18(3):188-190. (综述)
22) 瞿金涛,汪玫,肖 林(通讯作者),Th17在多发性硬化中发病机制及相关治疗进展,中国实用医药杂志,2010,5(17):229-232. (综述)
23) 瞿金涛,汪玫,肖 林(通讯作者),T细胞在多发性硬化发病机制中作用的研究进展,国际免疫学杂志,2010,33(5):356-359. (综述)
24) 周海洋,肖 林(通讯作者),陈宜张: 盐皮质激素的非基因组作用及其机制,生理科学进展,2008,39(1):45-48 (综述)
25) 肖 林(通讯作者),周海洋,戴若以,陈宜张: 糖皮质激素基因组作用及其生物学意义,中华内分泌道谢杂志,2007,23(3): 280-283. (综述)
26) 肖 林, 邱俭, 孙刚, 陈宜张*: 雌激素在中枢神经系统中的作用。 生理科学进展, 2001, 32(1):27-30.(综述)
27) 肖 林, 由振东,何成*,研究生神经生物学教学改革初探,山西医科大学学报基础医学教育版,2010 <span style="color: black; font-family